
中国学者表现卓越,共有近百篇研究入选口头报告(占全球口头报告总数12%),其中中青年学者占比超过60%,中国学者论文发表数量居全球第二,仅次于美国; “中国之夜”主题活动顺利举行,逾150位华人专家与学者共聚一堂,集中展示包括血友病A基因治疗产品GS1191-0445在内的多个中国原研药物的领先进展,吸引超过300位国际学者参与交流; 在创新药物领域中国成果显著,华毅乐健GS1191-0445注射液等多个差异化血液治疗产品披露最新临床试验数据,涵盖白血病、淋巴瘤、骨髓瘤等疾病的突破性治疗方法; 中国主导的国际多中心研究首次于ASH主会场进行口头报告,体现了中国在血液学领域从“参与”到“引领”的重要转变,显著提升了中国在国际血液学界的影响力。
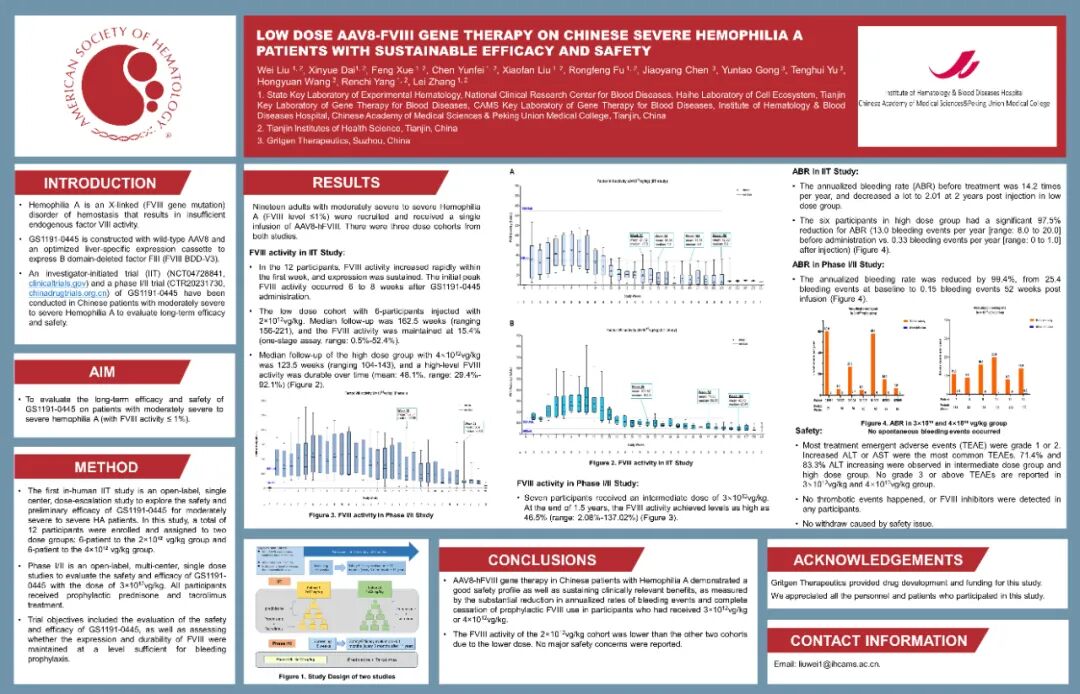
2021年启动研究者发起临床研究(IIT); 2023年1月获中国国家药监局批准开展Ⅰ期临床试验,同年8月完成首例患者给药; 2023年12月获美国FDA授予孤儿药资格认定; 2025年4月正式进入Ⅲ期临床研究; 2025年4月被中国国家药品监督管理局药品审评中心(CDE)纳入突破性治疗品种,上市进程稳步推进。
关于华毅乐健









