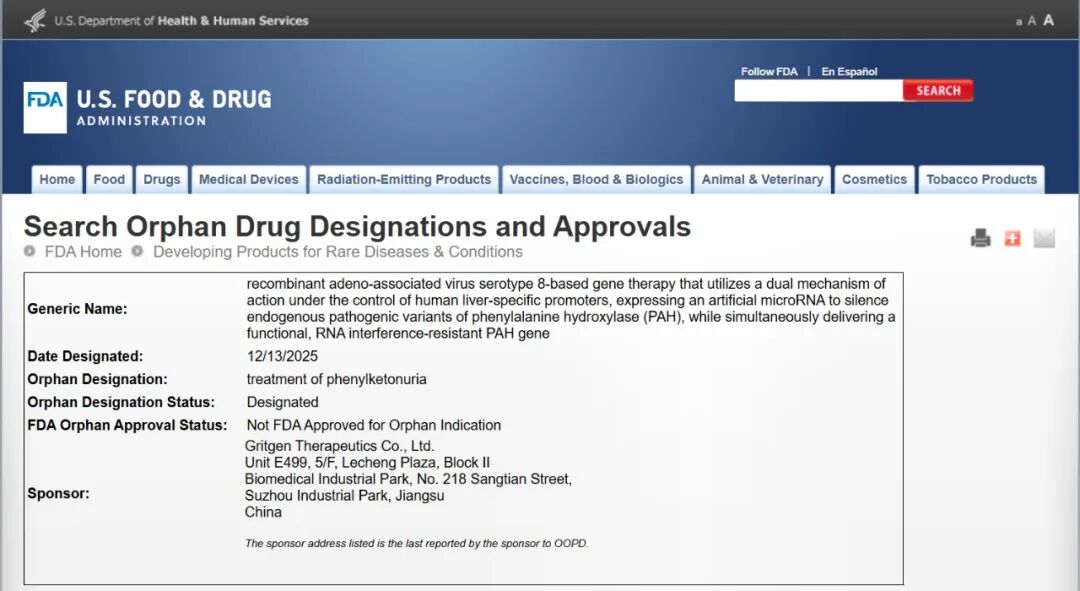
2025年12月13日,华毅乐健自主研发的GS1168注射液,一种针对苯丙酮尿症(PKU)的基因疗法,成功获得了美国食品药品监督管理局(FDA)的孤儿药资格认定(ODD)。
这一成就不仅代表了GS1168注射液研发进程中的一个重要里程碑,也为全球PKU患者带来了改变疾病进程的新机遇。

华毅乐健


我们非常重视您的个人隐私,当您访问我们的网站时,请同意使用的所有cookie。有关个人数据处理的更多信息可访问《隐私条款》
2025年12月13日,华毅乐健自主研发的GS1168注射液,一种针对苯丙酮尿症(PKU)的基因疗法,成功获得了美国食品药品监督管理局(FDA)的孤儿药资格认定(ODD)。
这一成就不仅代表了GS1168注射液研发进程中的一个重要里程碑,也为全球PKU患者带来了改变疾病进程的新机遇。


华毅乐健

